천연 항균성분 함유 콘택트렌즈의 제조 및 용출 특성

초록
본 연구에서는 소프트콘택트렌즈(이하 소프트렌즈)를 천연 항균성분의 전달시스템으로 사용하고 최적화된 약물 방출이 가능한 렌즈합성 조건을 제시하고자 하였다.
천연 항균성분으로 글리시리진산 암모늄염을 사용하였고, 이의 농도를 달리하여 분자각인법으로 소프트렌즈를 합성하고, 합성된 렌즈로부터 방출되는 글리시리진산의 양을 측정하여 방출 양상을 기능성 모노머의 개수와 개시제의 농도 별로 비교하였다.
글리시리진산의 농도가 증가할수록 약물이 로딩될 수 있는 공간 확보가 가능하였고, 0.05 mM의 로딩으로도 높은 방출 효율을 나타내었다. 또한 0.5%의 개시제 농도에서 단일 기능성 모노머를 사용하였을 때 글리시리진산의 총 방출량이 가장 큰 것으로 나타났으며, 다 기능성 모노머를 사용하였을 때에는 초기 방출량이 적을 뿐만 아니라 상대적으로 일정한 속도로 방출이 지속됨을 확인하였다.
본 연구 결과 글리시리진산을 함유하는 소프트렌즈 합성조건의 확립이 가능하였으므로 기존 항생제가 가지는 균에 대한 내성문제를 해결할 수 있으며, 포도상구균 등 안질환을 일으키는 균을 억제하는 기능성 소프트렌즈의 개발이 가능하리라 생각된다.
Abstract
This study aimed to implicate a lens synthesis process that uses soft contact lenses (hereinafter soft lenses) as a drug delivery system for a natural antibacterial component and allows optimal release of the drug.
Glycyrrhizic acid ammonium salt was used as a natural antibacterial component, and it was added to the synthesized soft lenses using molecular imprinting polymerization (MIP). The amount released from the synthesized lenses was measured and compared according to the number of functional monomers and initiator concentration.
As the concentration of glycyrrhizic acid increased, it was possible to make greater space for the drug to be loaded, and the loading amount of 0.05 mM showed high efficiency with respect to its release. When applying the MIP technique, it was found that the total release of glycyrrhizic acid was highest when a single functional monomer was used with a 0.5% concentration of the initiator, and when multifunctional monomers were used, the release was prolonged at a relatively constant rate as well as having a low initial burst release.
This study shows that it is possible to establish the conditions for synthesizing soft lenses containing glycyrrhizic acid, thus solving the resistance issue facing current antibiotics and developing a functional soft contact lens that inhibits ocular disease caused by bacteria such as Staphylococcus aureus.
Keywords:
Soft contact lenses, Molecular imprinting polymerization technique, Natural product, Anti-bacterial activity, Drug release키워드:
소프트콘택트렌즈, 분자각인법, 천연물질, 항균작용, 약물방출서 론
소프트콘택트렌즈(이하 소프트렌즈)는 착용 시 각막에 직접 접촉되기 때문에 착용자의 소홀한 관리,[1] 잘못된 착용 등의 이유로 각막궤양, 각막염과 같은 감염의 부작용이 발생될 수 있다.[2,3] 콘택트렌즈 착용으로 발생할 수 있는 안구감염은 세균, 진균 및 바이러스 등의 원인으로 나타날 수 있으며, 포도상구균과 녹농균에 의한 세균성 각막염의 빈도가 가장 높은 것으로 알려져 있다.[4,5] 감염의 치료는 대부분 약물을 통하여 이뤄지게 되며 안구로 약물을 전달시키는 방법으로 안구 내 주사, 안약 및 안 연고 등의 사용이 있으나 일반적으로 가장 많이 사용되는 방법은 안약의 점안이라 할 수 있다.[6] 안약의 점안은 약물전달 방법 중 가장 간단하다는 장점이 있으나 눈물 순환, 눈물관을 통한 배출 등으로 인하여 5% 미만의 생체이용률을 나타내어 매우 낮은 흡수율을 보이고 있다.[7-9] 이러한 안약의 문제점을 해결하기 위해서 약물전달 매개체로 소프트렌즈를 이용한 방법이 제시되었고,[10] 콘택트렌즈에 약물을 함유시킨 후 방출되도록 하는 연구가 최근까지도 활발하게 진행되고 있다.[11-16]
또한 기존 약물을 사용하는 연구에서는 약물에 대한 내성문제 및 높은 농도의 사용으로 인한 부작용 등의 한계를 가지고 있어[17-19] 이를 대체하고자 오랜 임상결과가 축적된 천연물질 중에서 감염을 방지할 수 있는 항균성분을 찾으려는 노력이 이루어지고 있다.[20] 여러 선행연구 결과, 한방이나 민간에서 널리 사용되는 천연물인 감초가 항균력을 가지는 성분을 함유하고 있는 것으로 보고된 바 있다.[20-22] 감초의 대표적인 성분인 글리시리진산은 트리테르페노이드계 물질로 감초 뿌리에 3~5% 정도 함유되어 있으며, 항균작용 뿐만 아니라 항산화, 항바이러스 및 항궤양 작용 등 다양한 약리작용을 가지므로 의약품, 식품, 화장품 등에도 사용되고 있다.[23] 최근에는 글리시리진산이 몇몇 코르티코스테로이드와 유사한 활성을 가지는 것으로 확인되었고, 추출물 또한 항염증 효과와 무기질코르티코이드 유사 활성을 가지는 것으로 보고됨에 따라 염증반응을 치료하기 위한 연구도 진행되고 있다.[24]
이에 본 연구에서는 대표적인 천연 항균물질인 글리시리진산을 목표 약물로 선정하고, 약물전달 매개체로 소프트렌즈를 이용하여 항균력을 가진 치료용 소프트렌즈를 개발하고자 하였다. 즉, 글리시리진산의 항균력을 평가하고 최적의 농도로 안구로 방출되도록 하는 콘택트렌즈의 제조 조건을 제시함으로써 새로운 치료용 소프트렌즈로 사용될 수 있는 가능성을 높이고자 하였다.
대상 및 방법
1. 재료
소프트렌즈 합성을 위하여 기본 모노머로 HEMA(2-hydroxyethyl methacrylate, Junsei, Japan) 및 MAA(methacrylic acid, Sigma-Aldrich, USA), 교차결합제인 EGDMA(ethylenglycol dimethacrylate, Sigma-Aldrich, USA), 열개시제인 AIBN(azobisiobutyonitile, Sigma-Aldrich, USA)와 습윤성을 위한 기능성 모노머로 NVP(N-vinyl pyrrolidone, Junsei, Japan)를 사용하였으며, 감초 성분 중 하나인 글리시리진산 암모늄염(glycyrrhizic acid ammonium salt from Glycyrrhiza root, ≥70%, Sigma-Aldrich, USA)을 사용하였다.
2. 글리시리진산 및 합성된 소프트렌즈의 항균 성능 평가
글리시리진산 함유의 합성 소프트렌즈에 대한 항균력은 ISO 기준(ISO 14729)[25]에 따라 검사하였다. 항균력 측정을 위하여 포도상구균(Staphylococcus aureus, ATCC 6548)을 한국미생물 보존센터(Korean Culture Center of Microorganisms, KCCM)에서 구입하여 사용하였고, Tryptone soy broth(Becton, Dickinson and Company, USA) 배지를 사용하여 배양하였다.
Tryptone soy broth에 0.08 w/v%의 Bacto agar(Becton, Dickinson and Company, USA)를 추가하여 semi agar의 형태로 균 배양 배지를 만든 후 루프를 이용하여 균을 도말하고 35~37oC의 온도에서 18~24시간 동안 배양시켰다. 1.0×104 cfu/mL의 희석균 1 mL를 멸균된 1.5 mL 튜브에 넣고 원심분리(13,500 rpm, 1 min)한 후 상층액을 제거하였다. 침전물 상태의 균에 0.004, 0.007, 0.014, 0.06 및 0.23 mM 농도의 글리시리진산 용액 1 mL을 넣어 1시간 동안 노출시킨 후 다시 13,500 rpm으로 원심분리하여 상층액을 제거하고 침전물 상태의 균에 인산완충용액(phosphate buffer saline, PBS, pH 7.4) 1 mL를 넣어 배지에 100 μL을 도말한 후 동일한 같은 배양조건에서 배양한 후 균 수를 측정하였다.
글리시린진산 함유의 소프트렌즈의 항균력 측정을 위하여 멸균된 12-well plate에 1.0×105 cfu/mL의 포도상구균 10 μL를 넣은 후 글리시리진산 농도를 각각 0.1, 1 및 2 mM로 공중합하여 렌즈 전면이 plate의 바닥에 닿게 놓고, 다시 10 μL의 균을 렌즈 위에 올리고 10분간 흡착시켰다. 균이 흡착된 렌즈를 PBS가 담겨있는 12-well plate에서 3번 헹구고 여과장치에 올려놓고 3분 동안 유지시킨 후 여과시켰다. 여과시킨 렌즈는 새 plate에 렌즈 전면이 접촉하도록 올린 후 Tryptone soy agar(Becton, Dickinson and Company, USA)를 부어 굳혔다. 항균력은 1일 뒤 자란 균 수를 측정하여 평가하였다.
3. 글리시리진산 로딩을 위한 소프트렌즈의 합성
기본 모노머에 글리시리진산을 1, 25, 33.3 및 50 mM의 농도로 첨가한 후 오븐(Wise oven, DAIHAN scientific, Korea)에서 100oC, 40분 동안 열중합하여 소프트렌즈를 주형주조 공법으로 0.00 D의 소프트렌즈를 제조하였다(Table 1).
합성된 소프트렌즈는 3차 증류수에 24시간 동안 수화시킨 후 0.1 Mpa, 121oC의 증기(Wise clave, DAIHAN scientific, Korea)에서 20분 동안 반응시켜 렌즈 내 남아있는 글리시리진산을 방출시켜 이후 약물이 로딩될 수 있는 공간이 확보되도록 하였다. 이러한 분자각인법(molecular imprinting polymerization)으로 합성한 소프트렌즈를 0.05 mM 글리시리진산이 함유된 PBS가 담긴 바이알에 48시간 동안 담구어 약물이 충분히 로딩되도록 하였다.
또한 최적화된 글리시리진산의 방출조건을 확립하기 위하여 기능성 모노머로 NVP를 추가하고 개시제인 AIBN의 양을 0.12, 0.25, 0.5 및 1.0 v/v%로 달리하여 상기와 동일하게 분자각인법으로 렌즈를 합성하고 글리시리진산을 로딩하였다(Table 2).
4. 글리시리진산의 로딩량 및 방출량 측정
합성된 소프트렌즈로부터의 글리시리진산 방출은 ISO 규격에 따라 PBS[26]를 용매로 사용하였다. 합성된 소프트렌즈를 PBS 5 mL이 담긴 바이알에 넣고 진탕기(Shaker, CR300, FINE-PCR, Korea)를 이용하여 50 rpm의 속도로 연속적으로 진탕하여 약물이 방출되도록 하였고, 각 바이알에서 PBS 1 mL를 취하여 분광도계(Mega array, SINCO, Korea)를 이용하여 254 nm에서 1, 2, 4, 6, 8, 24 및 168시간 동안의 흡광도를 측정하였다. 방출된 약물의 농도는 전체 방출량 대비 각 시간 당 방출된 약물의 농도를 계산하여 yield(%)값으로 나타내었다.
결과 및 고찰
1. 글리시리진산의 항균력
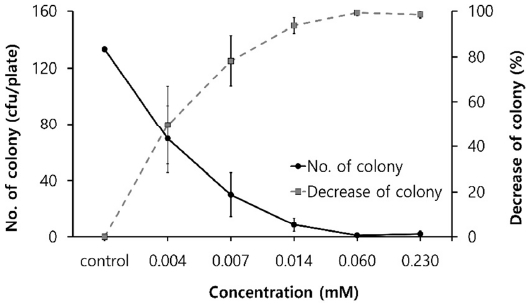
글리시리진산이 없는 PBS가 첨가된 대조군을 24시간 배양하였을 때 측정된 포도상구균 콜로니 수는 평균 133±18.4 cfu/plate이었다. 반면 글리시리진산의 농도가 0.004, 0.007, 0.014, 0.06 및 0.23 mM일 때, 포도상구균의 콜로니 수는 순서대로 69.3±23.8, 30.0±15.3, 8.6±4.7, 1.0±1.7 및 2.0±2.0 cfu/plate로 나타났다. 이를 균 수 감소율로 계산한 결과 각각 49.5, 78.1, 93.6, 99.2 및 98.4%로 나타나 약물의 농도가 높을수록 높은 항균력을 가짐을 확인하였고, 0.06 mM 이상 글리시리진산의 항균력은 크게 차이가 없음을 알 수 있었다(Fig. 1).
글리시리진산의 항균력에 대한 Zhoa 등[27]의 선행연구에서 0.25 mM의 낮은 글리시리진산이 포도상구균에 대한 항균력을 나타냈으며, 농도가 증가할수록 더 큰 항균력을 보였고, 특히 1.5 mM에서 포도상구균의 성장을 완전히 억제할 수 있다고 보고한 바 있어 글리시리진에 대한 본 연구 결과와 유사한 양상을 보였다.
한편, 글리시리진산과 HEMA를 열중합하여 제조된 소프트렌즈에 도포한 포도상구균에 대한 항균력을 알아보았다. 글리시리진산이 함유되어 있지 않은 대조군에서의 포도상구균 수는 27.7±3.1 cfu/lens이었고, 글리시리진산 농도가 각각 0.1, 1 및 2 mM인 소프트렌즈에서의 포도상구균 수는 각각 7.0±3.0, 0.0±0.0 및 1.3±0.7 cfu/lens이었다. 대조군을 기준으로 하여 포도상구균의 감소율은 각각 74.7, 99.9 및 95.9%이었다(Fig. 2A). 또한, 시간에 따른 글리시리진산의 방출은 0.1과 1 mM 모두 초기 8시간 이내에 50% 이상의 방출을 보였다(Fig. 2B).
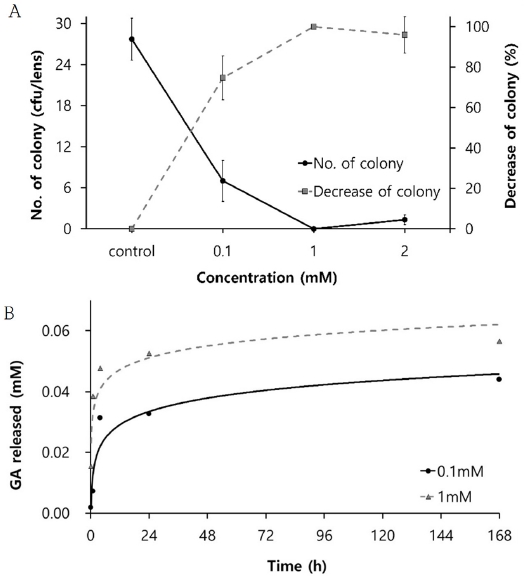
Antibacterial activity of glycyrrhizic acid-laden contact lens against Staphylococcus aureus.A. Number of colonies and reduction ratio of Staphylococcus aureusB. Concentration of glycyrrhizic acid released from polymerized soft lenses
따라서 글리시리진산을 1 mM 농도로 중합한 소프트렌즈에서 포도상구균에 대한 가장 높은 항균력이 있음을 알 수 있었으며, 포도상구균에 대한 항균력을 가지는 소프트렌즈의 합성 가능성을 확인할 수 있었다. 그러나 초기 8시간 이내에 50% 이상의 방출량을 보이는 것으로 보아 고농도를 사용했을 때 문제가 될 수 있어 소프트렌즈 합성 방법을 분자각인법으로 전환하였다.
2. 분자각인법으로 합성된 소프트렌즈로부터 글리시리진산 방출 양상
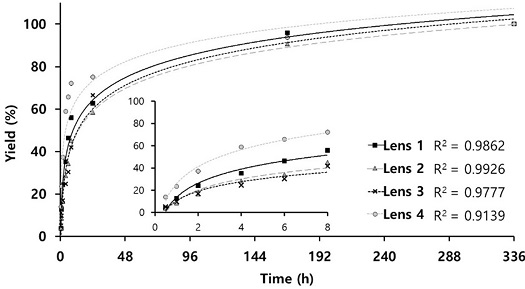
분자각인법을 사용하여 합성한 소프트렌즈를 약물전달 매개체로 작용하기 위하여 가장 효율적으로 방출될 수 있는 글리시리진산의 농도를 설정하고자 각각 1, 25, 33.3 및 50 mM의 농도로 로딩하여 PBS에서 방출되도록 한 후 30분, 1, 2, 4, 6, 8, 24, 168 및 336시간에 측정된 글리시리진산의 농도를 누적하여 총 방출량으로 나타내었다.
1, 25, 33.3 및 50 mM 농도로 글리시리진산과 HEMA를 열중합하였을 때 8시간 동안의 초기 방출량(Fig. 3 내 삽입 그래프)은 각각 0.016, 0.014, 0.014 및 0.029 mM이었고, 336시간 동안의 총 방출량(Fig. 3)은 각각 0.028, 0.032, 0.033 및 0.040 mM로 나타났다. 중합한 글리시리진산의 농도에 관계없이 시간 의존적으로 방출량은 증가하는 것으로 나타났으나(all R2 > 0.9100), 글리시리진산의 초기 및 총 방출량 모두 50 mM의 농도로 중합된 Lens 4에서 가장 크게 나타났다. 이를 렌즈 별로 336시간 동안의 총 방출량 대비 누적 비율(yield %)로 나타내었을 때, Lens 1, 2, 3 및 4에서 각각 55.94, 45.13, 41.86 및 72.20%로 나타나 Lens 4에서 가장 높은 방출 효율을 보임을 알 수 있었다.
3. 기능성 모노머 사용에 따른 소프트렌즈로부터 글리시리진산의 방출 양상
글리시리진산을 열중합하여 제조한 항균 소프트렌즈로부터 가장 많은 약물 방출량과 높은 방출 효율을 보인 50 mM의 글리시리진산을 기준으로 하여 약물농도를 일정하게 유지한 상태에서 기능성 모노머로 NVP를 사용하면서 개시제 비율의 변화에 따라 글리시리진산의 방출에 어떠한 영향을 미치는가를 알아보고자 하였다.
NVP를 사용하지 않고, HEMA와 AIBN의 구성 비율을 조정하여 합성한 경우를 단일 기능성 모노머 사용, NVP를 사용하면서 HEMA와 AIBN의 구성 비율을 조정한 경우를 다 기능성 모노머 사용으로 분류하였고, 단일 혹은 다 기능성 모노머를 사용한 소프트렌즈로부터 글리시리진산이 방출된 축적 농도를 시간 별로 알아보았다(Fig. 4).
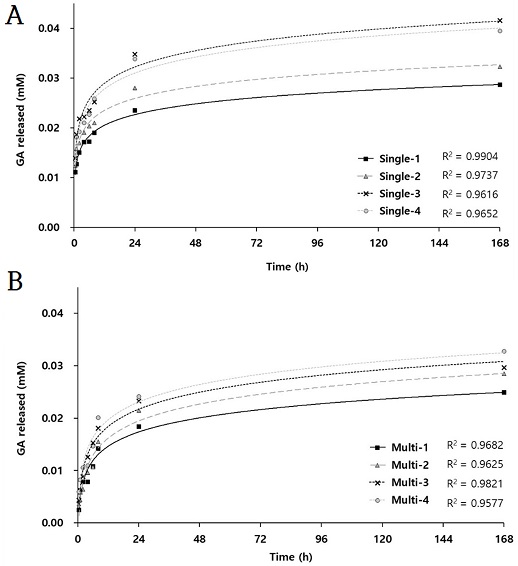
Concentration of glycyrrhizic acid released from soft lenses polymerized with single- or multifunctional monomer(s).
개시제인 AIBN의 농도가 0.12, 0.25, 0.5 및 1.0%일 때, 단일 기능성 모노머를 사용하여 합성했을 경우 글리시리진산 방출량은 각각 0.029, 0.032, 0.042 및 0.039 mM이었고, 다 기능성 모노머의 경우에는 각각 0.025, 0.029, 0.030 및 0.033 mM로 나타났다. 모든 개시제 농도 비율에서 단일 기능성 모노머를 사용했을 때 글리시리진산의 총 방출량이 다 기능성 모노머의 경우보다 더 큰 것으로 나타났으며, 특히 0.5% 개시제 비율로 단일 기능성 모노머를 사용하였을 때 방출량이 가장 큰 것으로 확인되었다.
이를 단일 혹은 다 기능성 모노머 사용 시 글리시리진산의 방출 효율로 비교하여 개시제의 비율에 따라 168시간 동안의 총 방출량 대비 누적 비율(yield %)로 계산하여 보았다(Fig. 5).
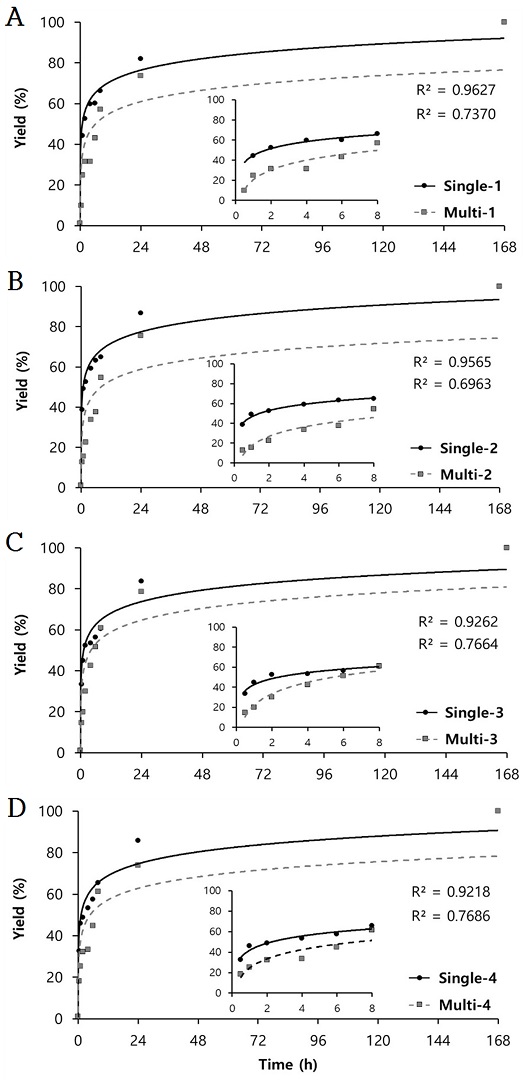
Yield of glycyrrhizic acid released from soft lenses polymerized with single- or multifunctional monomer(s) and different ratios of AIBN.A. Comparison of single- and multifunctional monomers with 0.12% initiatorB. Comparison of single- and multifunctional monomers with 0.25% initiatorC. Comparison of single- and multifunctional monomers with 0.5% initiatorD. Comparison of single- and multifunctional monomers with 1.0% initiator
개시제 비율이 0.12, 0.25, 0.5 및 1.0%일 때 단일 기능성 모노머를 사용한 렌즈의 초기 8시간 동안의 방출 효율은 각각 66.28, 64.92, 60.53 및 65.51%로 나타났으며, 다 기능성 모노머를 사용한 경우 각각 57.06, 54.59, 60.91 및 61.30%의 방출량을 보였다. 단일 기능성 모노머를 사용했을 때에는 초기 2시간 만에 50% 이상의 글리시리진산이 과다하게 방출된 것으로 나타났던 반면, 다 기능성 모노머를 사용한 경우에는 8시간이 경과하였을 때 50%의 방출이 일어나 비교적 안정적인 약물 방출이 이루어졌음을 확인할 수 있었다.
콘택트렌즈 합성 시 고분자인 모노머 사이의 크기는 다양한 요소들에 영향을 받게 되는데 이 공극 크기는 소프트렌즈의 함수율과 산소투과도 뿐만 아니라 약물전달 매개체로 사용될 때 약물 전달속도에 영향을 미치게 된다. 소프트렌즈로부터 방출되는 약물의 용출속도를 조절하는 방법 중에는 고분자의 입자 크기 조절과 약물 자체의 성질을 이용하는 방법이 있다.[28,29] 특히 소프트렌즈의 모노머의 구성 중 개시제는 중합 시 필수 화합물로서 농도가 높을 경우 고분자 사슬의 길이가 길어지는 특징을 가지고 있어 고분자 사슬 길이나 입자 크기의 조정을 위해 개시제의 농도를 조절하게 된다.[30] 본 연구 결과에서도 개시제의 양이 증가함에 따라 글리시리진산의 총 방출량이 증가하는 양상을 보였는데 이는 노플록사신 약물을 이용하여 개시제 양을 변화하여 약물 방출 프로필을 본 박 등[16]의 연구에서 개시제의 양이 증가할수록 약물 방출량도 많아진다는 결과와 유사하다. 선행연구에 사용된 노플록사신의 분자량은 319.33 g/mol로 839.96 g/mol의 글리시리진산의 분자량보다 작음에도 불구하고 약물침지법(soaking) 보다 분자각인법으로 약물을 로딩하였을 때 로딩된 약물의 농도가 높고, 방출 지속시간이 긴 것으로 나타났으므로, 글리시리진산의 경우에는 더 긴 고분자 사슬 길이가 요구될 것으로 예상할 수 있었고, 본 연구 결과 분자각인법이 실제로 글리시리진산의 로딩과 방출에 기여한 것으로 생각되었다.
또한 단일 및 다 기능성 모노머를 사용한 방출 프로필의 비교에서 다 기능성 모노머 사용 시 방출 시간이 길어짐을 확인할 수 있었는데 이는 사용된 모노머 간의 상호작용과 연관이 있을 것으로 생각되었다. 다 기능성 모노머를 사용하여 오플록사신과 네오마이신의 방출량을 확인한 이 등[31]의 연구에서는 기능성 모노머의 비율이 증가할수록 방출량도 증가하였다고 보고한 바 있는데, 본 연구에서도 기능성 모노머의 비율이 증가하였을 때 글리시리진산의 방출량이 큰 것으로 나타났다. 본 연구에서 기능성 모노머로 사용된 MAA와 NVP는 친수성 모노머로, HEMA를 기본 모노머로 하는 소프트렌즈에서 함수율을 높이기 위해 사용된다. 기능성 모노머의 친수성이 높아질수록 약물의 로딩양도 증가한다는 다른 선행연구 결과에서와 마찬가지로 본 연구에서도 하이드로겔 체인의 친수성이 향상됨과 동시에 약물과 하이드로겔 사이 정전기적 상호작용으로 인하여 약물의 로딩 및 방출량이 증가하였던 것으로 생각된다. 여러 연구를 통해 고분자 네트워크에 분자각인법 방식을 적용시킬 경우 약물 로딩 능력이 향상되며[15] 약물과 기능성 모노머의 비율을 조절한다면 약물 방출 기간을 지속시킬 수 있다는 연구가 보고된 바와 마찬가지로[16] 글리시리진산의 항균력과 약물 방출 기간을 증가를 위해서 약물 로딩 방법과 기능성 모노머의 비율 조절이 중요함을 알 수 있었다.
본 연구 결과 항균력을 가지는 글리시리진산을 함유한 소프트렌즈를 합성하고 효율적인 방출 양상을 보이는 합성조건을 제시할 수 있었으나 방출을 지속하는 데에 있어 속도를 고려하여야 할 필요가 있는 것으로 생각되었다. 약물전달 매개체로써 소프트렌즈를 사용하는 것은 약물농도의 큰 변동없이 오랜 시간 일정한 농도로 전달하는 데에 목적을 가지고 있다. 그러나 콘택트렌즈를 이용한 약물전달에서 과다한 초기 방출에 대한 문제점이 지속적으로 제시되고 있고, 이를 해결하고자 하는 많은 시도가 있었다. 본 연구에서는 단일 기능성 모노머를 사용한 소프트렌즈와 2개 이상의 다 기능성 모노머를 사용한 소프트렌즈의 합성이 수행되었고, 방출 양상의 비교 시 총 방출량에서는 단일 모노머를 사용했을 때 더 큰 값을 나타내었으나, 시간 당 방출량을 보면 다 기능성 모노머를 사용한 소프트렌즈에서 약물 방출이 급격하지 않은 기울기의 초기 방출 속도를 나타내었다. 따라서 단기간 항균 치료를 위한 경우라면 초기 방출량이 많았던 단일 기능성 모노머 기반의 소프트렌즈를 사용이 유용할 것으로 예상되며, 지속적인 약물방출이 요구되는 경우라면 다 기능성 모노머 기반의 소프트렌즈를 약물전달 매개체로 사용할 필요가 있다고 판단되었다.
또한 본 연구 결과를 통해서 글리시리진산을 함유하는 소프트렌즈의 화학적, 생물학적 안정성은 확인할 수 있었다. 그러나 소프트렌즈의 물리학적 및 광학적 성능 등 시력 교정을 위하여 기본적으로 요구되는 렌즈 파라미터들에 대해서는 확인하지 못하여 이에 대한 추가적인 연구가 필요할 것으로 생각된다.
결 론
본 연구에서는 글리시리진산을 활용하여 항균력을 가진 소프트렌즈를 개발하고자 하였다. 글리시리진산의 효율적인 로딩을 위하여서는 공중합 방식보다는 단일 혹은 다기능성 모노머를 사용하여 분자각인법으로 글리시리진산을 함유하도록 소프트렌즈를 제조하였을 때 보다 낮은 약물 농도에서도 포도상구균에 대한 항균력을 가지는 것으로 확인되었다. 또한 다 기능성 모노머를 사용하여 분자각인법으로 글리시리진산을 소프트렌즈 내로 로딩하였을 때 소프트렌즈로부터 초기의 글리시리진산의 방출을 낮출 수 있는 것으로 확인되었다. 따라서 글리시리진산을 함유한 소프트렌즈는 기존 항생제가 가지는 균에 대한 내성문제를 해결할 수 있으며, 포도상구균 등 안질환을 일으키는 균을 억제하는 기능성 소프트렌즈로 활용될 수 있을 것이다.
References
-
Boost M, Poon KC, Cho P. Contamination risk of reusing daily disposable contact lenses. Optom Vis Sci. 2011;88(12): 1409-1413.
[https://doi.org/10.1097/OPX.0b013e3182346616]

-
Kim TH, Sung AY. Physical characterization and contact lens application of polymer produced with propylene glycol additive. J Korean Chem Soc. 2010;54(1):105-109.
[https://doi.org/10.5012/jkcs.2010.54.01.105]

-
Suchecki JK, Donshik P, Ehlers WH. Contact lens complications. Ophthalmol Clin N Am. 2003;16(3):471-484.
[https://doi.org/10.1016/S0896-1549(03)00056-7]

-
Green M, Apel A, Stapleton F. Risk factors and causative organisms in microbial keratitis. Cornea. 2008;27(1):22-27.
[https://doi.org/10.1097/ICO.0b013e318156caf2]

-
Park SH, Park I, Kim SR, et al. Relationship between the deposition of tear constituents on soft contact lenses according to material and pigmentation and adherence of staphylococcus aureus. J Korean Ophthalmic Opt Soc. 2016;21(2): 109-117.
[https://doi.org/10.14479/jkoos.2016.21.2.109]

- Kumar A, Malviya R, Sharma PK. Recent trends in ocular drug delivery: a short review. European J Appl Sci. 2011; 3(3):86-92.
-
Kearns VR, Williams RL. Drug delivery systems for the eye. Expert Rev Med Devices. 2009;6(3):277-290.
[https://doi.org/10.1586/erd.09.4]

-
Rad MS, Mohajeri SA. Extended ciprofloxacin release using vitamin E diffusion barrier from commercial silicone-based soft contact lenses. Eye Contact Lens. 2017;43(2): 103-109.
[https://doi.org/10.1097/ICL.0000000000000245]

-
Nikouei BM, Vahabzadeh SA, Mohajeri SA. Preparation of a molecularly imprinted soft contact lens as a new ocular drug delivery system for dorzolamide. Curr Drug Deliv. 2013;10(3):279-285.
[https://doi.org/10.2174/1567201811310030004]

- Sedlacek J. Possibility of the application of ophthalmic drugs with the use of gel contact lenses. Cesk Oftalmol. 1965;21(6):509-512.
-
Kim G, Lee J, Noh H. Study of drug release from hydrogel contact lens containing coacervated drugs. Polymer (Korea). 2018;42(3):427-433.
[https://doi.org/10.7317/pk.2018.42.3.427]

-
Silva D, de Sousa HC, Gil MH, et al. Imprinted hydrogels with LbL coating for dual drug release from soft contact lenses materials. Mater Sci Eng C. 2021;120:111687.
[https://doi.org/10.1016/j.msec.2020.111687]

-
Raesian P, Rad MS, Khodaverdi E, et al. Preparation and characterization of flouorometholone molecular imprinted soft contact lenses as ocular controlled drug delivery systems. J Drug Deliv Sci Technol. 2021;64:102591.
[https://doi.org/10.1016/j.jddst.2021.102591]

-
Pereira-da-Mota AF, Vivero-Lopez M, Topete A, et al. Atorvastatin-eluting contact lenses: effects of molecular imprinting and sterilization on drug loading and release. Pharmaceutics. 2021;13(5):606.
[https://doi.org/10.3390/pharmaceutics13050606]

-
Kang DY, Kwon GW, Jung KH, et al. Drug-release performance of acrylic hydrogel membranes synthesized using a novel cross-linker. Polymer(Korea). 2016;40(4):628-634.
[https://doi.org/10.7317/pk.2016.40.4.628]

-
Park H, Lee HM. Changes in drug elution concentration and physical characteristics of soft contact lenses depending on the initiator and crosslinker. J Korean Ophthalmic Opt Soc. 2014;19(2):145-151.
[https://doi.org/10.14479/jkoos.2014.19.2.145]

-
Stone JL, Robin AL, Novack GD, et al. An objective evaluation of eye drop instillation in patients with glaucoma. Arch Ophthalmol. 2009;127(6):732-736.
[https://doi.org/10.1001/archophthalmol.2009.96]

-
Lomaestro BM. Fluoroquinolone-induced renal failure. Drug Saf. 2000;22(6):479-485.
[https://doi.org/10.2165/00002018-200022060-00006]

-
Frishman WH, Kowalski M, Nagnur S, et al. Cardiovascular considerations in using topical, oral, and intravenous drugs for the treatment of glaucoma and ocular hypertension: focus on beta-adrenergic blockade. Heart Dis. 2001;3(6):386-397.
[https://doi.org/10.1097/00132580-200111000-00007]

-
Alvarez-Lorenzo C, Yañez F, Barreiro-Iglesias R, et al. Imprinted soft contact lenses as norfloxacin delivery systems. J Control Release. 2006;113(3):235-244.
[https://doi.org/10.1016/j.jconrel.2006.05.003]

-
Fenwick GR, Lutomski J, Nieman C. Liquorice, glycyrrhiza glabra L-composition, uses and analysis. Food Chem. 1990;38(2):119-143.
[https://doi.org/10.1016/0308-8146(90)90159-2]

-
Scherf A, Treutwein J, Kleeberg H, et al. Efficacy of leaf extract fractions of glycyrrhiza glabra L against downy mildew of cucumber(pseudoperonospora cubensis). Eur J Plant Pathol. 2012;134:755-762.
[https://doi.org/10.1007/s10658-012-0051-0]

-
Lee JM, Lee YM, Hur SS. Isolation and identification of antimicrobial compounds from licorice extracts. J Korean Oil Chem Soc. 2016;33(2):255-263.
[https://doi.org/10.12925/jkocs.2016.33.2.255]

-
Ahn SJ, Cho EJ, Kim HJ, et al. The antimicrobial effects of deglycyrrhizinated licorice root extract on Streptococcus mutans UA159 in both planktonic and biofilm cultures. Anaerobe. 2012;18(6):590-596.
[https://doi.org/10.1016/j.anaerobe.2012.10.005]

- ISO(International Organization for Standardization). Ophthalmic optics-contact lens care products-microbiological requirements and test methods for products and regimens for hygienic management of contact lenses, 2001. https://www.iso.org/obp/ui/#iso:std:iso:14729:ed-1:v1:en, (4 August 2021).
- ISO(International Organization for Standardization). Ophthalmic optics-contact lenses-part 3: Measurement methods 18369-3, 2017. https://www.iso.org/obp/ui/#iso:std:iso:18369:-3:ed-2:v2:en:enl, (4 August 2021).
-
Zhao X, Zhang H, Gao Y, et al. A simple injectable moldable hydrogel assembled from natural glycyrrhizic acid with inherent antibacterial activity. ACS Appl Bio Mater. 2020;3(1): 648-653.
[https://doi.org/10.1021/acsabm.9b01007]

-
Panyam J, Labhasetwar V. Biodegradable nanoparticles for drug and gene delivery to cells and tissue. Adv Drug Deliv Rev. 2003;55(3):329-347.
[https://doi.org/10.1016/S0169-409X(02)00228-4]

-
Oh KT, Bronich TK, Kabanov AV. Micellar formulations for drug delivery based on mixtures of hydrophobic and hydrophilic Pluronic block copolymers. J Control Release. 2004;94(2-3):411-422.
[https://doi.org/10.1016/j.jconrel.2003.10.018]

-
He J, Zhang H, Li C, et al. Effects of initiator homolysis rate constant on kinetics and chain length distribution in living free-radical polymerization. Polym J. 1999;31(7): 585-589.
[https://doi.org/10.1295/polymj.31.585]

-
Lee D, Lee N, Kwon I. Efficient loading of ophthalmic drugs with poor loadability into contact lenses using functional comonomers. Biomater Sci. 2018;6(10):2639-2646.
[https://doi.org/10.1039/C8BM00586A]