천연다당류와 칼슘이온이 네트워크된 다공성 콘택트렌즈의 특성

초록
천연 다당류 및 칼슘이온이 네트워킹된 다공성 콘택트렌즈를 제조하고 물성 변화를 조사하였다.
다공성 콘택트렌즈에 알지네이트와 히알루론산으로 네트워크화하고, 칼슘이온으로 2차 가교시켰다. 콘택트렌즈의 특성 평가는 함수율, 산소투과도, 접촉각, 인장강도, 표면분석, 단백질 흡착, 항균성 등을 측정하였다.
천연다당류를 첨가함으로써 콘택트렌즈의 습윤성, 단백질 흡착, 항균활성이 향상되었으며, 기계적 강도도 크게 향상되었다.
천연다당류와 칼슘이온을 이용하여 기능성이 향상된 다공성 하이드로겔 콘택트렌즈를 제조할 수 있었다.
Abstract
To manufacture porous contact lenses with natural polysaccharides and calcium ions and investigate changes in their physical properties.
Porous contact lenses were networked with alginate and hyaluronic acid, and secondarily cross-linked with calcium ions. The characteristics of the contact lenses were evaluated by measuring the water content, oxygen permeability, contact angle, tensile strength, surface analysis, protein adsorption, and antibacterial activity.
Addition of natural polysaccharides improved the wettability, protein adsorption, and antibacterial activity, and mechanical strength of the contact lenses.
Functionality of porous hydrogel contact lenses can be improved by adding natural polysaccharides and calcium ions.
Keywords:
Alginate, Hyaluronic Acid, Physical Property, Polysaccharide, Porous Contact Lens키워드:
다공성 콘택트렌즈, 히알루론산, 알지네이트, 다당류, 물리적 특성서 론
콘택트렌즈는 각막에 직접 착용하는 의료용품으로 재료의 물리적 특성 및 광학적 특성, 생체적합성, 무독성 등의 조건이 필요하며.[1] 재질과 디자인의 종류에 따라 각막에 미치는 영향이 달라지기 때문에 눈 건강에 중요하다. 이에 콘택트렌즈의 산소투과성과 습윤성 향상, 단백질 및 지질의 흡착 저하, 항균성 등 고기능성 콘택트렌즈에 대한 연구가 활발히 진행되고 있다.[2-4]
하이드로겔 콘택트렌즈는 유연하고 착용감이 좋은 장점을 가지기 때문에 많은 사람들이 선호하지만, 낮은 산소투과성으로 인한 각막 저산소증, 각막부종 등과 같은 문제점을 가지고 있다. 이에 하이드로겔 렌즈는 우수한 착용감을 유지하면서, 고습윤성과 높은 산소투과성이 요구되었다. 실리콘 모노머가 포함된 실리콘하이드로겔은 하이드로겔 콘택트렌즈보다 산소투과성은 향상되었지만, 렌즈표면의 소수성으로 인해 렌즈의 습윤성이 떨어지고 지질 및 단백질 등이 침착되어 착용감을 떨어지는 문제점을 가지고 있다.[5,6] 따라서 기존의 하이드로겔 콘택트렌즈가 가지는 낮은 산소투과성과 실리콘 하이드로겔 콘택트렌즈가 가지는 표면 습윤성의 저하와 같은 문제점을 보완할 수 있는 고기능성 콘택트렌즈 재질의 개발이 요구되고 있다.
최근에는 천연물질을 첨가하여 습윤성 및 함수율을 증가시키는 연구도 이루어지고 있다. 특히, 다당류는 생체 물질의 화학적 변형을 위해 가장 빈번하게 사용되는 천연 중 합체 중 하나로 카르복실 산 및 히드록실기의 존재로 인해 다른 물질과 반응을 쉽게 이룰 수 있어 매우 매력적인 소재로 사용되고 있다.[7-9] 히알루론산(HA)를 포함한 중합체는 습윤 또는 윤활작용으로 습윤성을 향상시키고 단백질 흡착을 감소시켜 콘택트렌즈의 전반적인 편안함을 향상시켰으며.[10,11] 알긴산을 포함한 중합체에서 습윤성의 향상으로 인해 단백질 부착을 감소시켰다.
천연 다당류를 이용한 하이드로겔이 생체 의학 및 약학 분야 등에서 많은 관심을 받고 있다.[12] 천연 다당류는 합성고분자에 비해 쉽게 모방 할 수 없는 다양한 조성과 특성을 가지고 있다.[13] 천연다당류 기반의 하이드로겔은 생체적합성, 생분해성, 다양한 생물학적 기능 등의 특성을 가지므로 응용분야가 다양해지고 있다.[14] 최근 들어 생의학 분야 및 제약으로 많이 사용되어지고 있는 다당류는 알긴산, 키토산, 덱스트란. 카라기난, 히알루론산 등이 있다.[15,16]
알긴산은 세포외 기질과 유사한 특성을 가지고 있으며, 생체적합성과 낮은 독성으로 인해 재생 의학 응용분야 및 조직 공학에 사용되기 적합한 물질이다.[17] 알긴산은 Ca2+와 같은 2가 금속이온에 대해 높은 친화성을 가지며 ‘egg box’형태를 이루게 된다.[18,19] 금속이온의 존재하에 형성된 알긴산 하이드로겔은 탄성 및 기계적 강도를 향상시키고 물리화학적 강도를 증가시켜 상처치유 드레싱 및 조직공학 응용에도 사용되고 있다.[20,21]
히알루론산은 하이드록시기(-OH)가 존재하여 수소결합을 통해 많은 양의 수분을 함유할 수 있으며, 수용액에서 안정적인 3차구조를 형성하여 보습능력이 뛰어난 소재로 알려져 있다. 또한 우수한 생체적합성과 생분해성으로 생의학 분야 및 산업에서 가장 많이 사용되는 고분자이다.[22,23]
본 연구에서는 눈 건강을 위한 고기능성 콘택트렌즈 개발을 위해 산소투과성과 습윤성이 높은 다공성 하이드로겔 콘택트렌즈를 제작하고, 천연다당류를 사용하여 콘택트렌즈의 물리적 특성을 향상시키고자 하였다. 또한 다공성 콘택트렌즈의 기계적 강도를 향상시키기 위하여 칼슘이온을 가교시켜서 콘택트렌즈의 특성을 살펴보고자 하였다.
대상 및 방법
1. 시약
콘택트렌즈의 제작에 사용한 시약은 2-hydroxy ethyl methacrylate(HEMA, JUNSEI), 가교제로 Ethylene glycol dimethacrylate(EGDMA, Aldrich), 개시제로 2,2-Azobisisobutyronitrile(AIBN, JUNSEI)을 사용하였으며, 캐스트몰드 방법으로 80oC에서 2시간 열중합하였다. 다공성 하이드로겔 제작은 발포제는 sodium carbonate(SC, Aldrich)를 사용하였으며, 발포반응을 위해 methacrylic acid(MAA, JUNSEI)을 사용하였다. 또한 상호침투 고분자 네트워크(Interpenetrating Polymer Network, IPN)를 위한 개시제는 ammonium persulfate(APS, Aldrich)와 교차결합제는 N,N'-methylenebisacrylamide(MBAA, Aldrich)을 사용하였다.
다공성 콘택트렌즈와 기준 콘택트렌즈 제작을 위한 구성성분비는 Table 1에 제시하였다.
2. 천연다당류와 칼슘이온이 가교된 다공성 콘택트렌즈 제작
천연다당류와 칼슘이온을 가교된 다공성 콘택트렌즈를 제작하기 위하여 알긴산과 히알루론산을 각각 1%, 0.5%의 용액으로 제조된 용액에 MBAA와 APS를 각각 0.3%씩 첨가하여 full-IPN으로 진행하였다. IPN은 천연 다당류를 녹인 각각의 용액에 콘택트렌즈를 37oC에서 24시간 동안 침지하였다. IPN을 진행한 다공성 콘택트렌즈 시료에 대한 명명은 Table 2에 제시하였다. IPN을 하지 않은 다공성 콘택트렌즈는 PC로 명명하였으며, 알긴산과 히알루론산으로 네트워크한 시료는 각각 PC-A, PC-H로 명명하였다. 한편 알긴산과 히알루론산 용액을 1:1의 비율로 혼합하여 네트워크한 시료는 PC-AH로 명명하였다.
다공성 하이드로겔의 인장강도를 높이기 위하여 염화칼슘(CaCl2)은 0.1M의 용액을 제조하여 각각의 시료를 10분 동안 침지시켰다.
3. 다공성 콘택트렌즈의 물리적 특성 평가 방법
함수율 측정은 ISO 18369-4:2006, Ophthalmic optics-Contact lenses-Part 4: Physicochemical properties of contact lens materials의 중량측정법(gravimetric method)을 사용하였다. PBS로 수화된 시료는 XS205 Dual Range(METTLER TOLEDO사, swiss)를 사용하여 한 시료 당 5개씩 무게를 측정하여 평균값으로 나타내었다.
산소전달률 측정은 ISO 18369-4:2006에서 제시한 Polarographic 방법으로 실시하였다. 실온에서 0.9% 생리식염수에서 24시간 이상 수화된 시료를 VL-50(Mitutoyo사, Japan)으로 중심 두께를 측정하였다. 시료는 온도 35oC, 습도 98%인 항온항습기 내부의 Flat cell에 고정하여 O2 PERMEOMETER_201T(Rehder사, USA)로 전류 값을 측정하였으며, 측정된 두께와 전류 값을 이용하여 Dk/t값으로 나타내었으며, 단위는 10−9(㎝·㎖O2)/(sec·㎖·㎜Hg)이다.
접촉각은 sessile drop 방법으로 제작한 콘택트렌즈를 실온에서 PBS에 24시간 이상 수화시킨 후 측정하였고, 초순수 증류수 3 ㎕를 콘택트렌즈 표면에 떨어뜨려 생성된 각도를 측정하였으며, 한 시료 당 1초당 2회씩 10초 동안 측정하여 평균하였다. 측정장비는 DSA30(Kruss GMBH사, Germany)을 사용하였다.
4. 다공성 콘택트렌즈의 단백질 정량
단백질 정량은 인간의 albumin과 형태 및 화학적 성질이 유사한 Sigma-Aldrich사의 소 혈청 알부민(Bovine Saline Albumin, BSA, 66.4kDa)을 사용하여 분광광도법으로 단백질 흡착 정도를 측정하였다.
단백질의 흡착 실험을 위해서 BSA와 라이소자임을 3 mg/ml 또는 5mg/ml를 PBS에 녹이고, 녹인 BSA용액 2 ml씩 바이알에 넣은 다음 각각의 시료를 37oC, 24시간 동안 인큐베이션하여 단백질을 흡착시켰다. 단백질 흡착시킨 시료를 꺼내 PBS로 2회 세정 후 3% Sodium Dodecyl Sulfate(SDS)용액이 담긴 바이알에 넣고 오븐에서 95oC로 15분간 가열 후 vortex로 3분간 천천히 흔들어 시료에 붙은 단백질을 탈착시켰다.
시료에 흡착되었던 단백질의 농도는 흡광계수를 이용한 방법을 사용하였으며,[24] 3% SDS 수용액을 base line으로 두고, 탈착시킨 단백질을 포함한 3% SDS 용액의 흡광도를 측정하였다. Agilent(USA)의 Cary 60 UV-vis를 사용하여 단백질의 흡수파장인 280 nm에서 흡광도 값을 측정하였다.
단백질 흡착량은 다음의 공식을 사용하여 계산하였으며, 단위는 mg/g을 사용하였다.
- Q is the protein adsorption amount.
- v is the volume of the solution.
- c is the protein concentration in the solution.
- m is the mass of the hydrated test specimens.
5. 다공성 콘택트렌즈의 인장강도 측정
압축강도의 측정은 AGS-X20N(SHIMADZU사, Japan)을 사용하였으며, 시험기의 지그는 콘택트렌즈를 고정시키기 위해 별도로 제작하였으며, 환봉을 사용하여 시험속도 10mm/min상태에서 측정을 하였다. 천연다당류에 IPN 하지 않은 시료는 실온에서 PBS에 24시간 이상 수화시킨 후 측정하였으며, 천연다당류에 IPN을 한 시료는 IPN 후 PBS에 2회 세척 후 측정하였다. 보푸라기가 없는 Wiper로 시료의 물기를 제거 한 후 측정하였으며, 각 시료 당 5개의 평균값을 나타내었다.
6. 다공성 콘택트렌즈의 표면분석
콘택트렌즈에 천연다당류와 칼슘이온을 결합시킨 시료의 표면분석을 위해 주사전자현미경(Scanning electron microscope, SEM)을 사용하였고, 측정 장비는 MIRA3(TESCAN사, USA)을 사용하여 분석하였다. 20 mA로 60초 동안 3.25 nm의 두께로 gold coating하여 측정하였다. 또한 LBL코팅을 진행한 콘택트렌즈의 표면 거칠기 정도를 확인하기 위해 원자힘현미경(Atomic Force Microscopy, AFM)을 사용하였다. 측정 장비는 NX10(Park systems사, Czech)의 을 사용하여 확인하였으며, 5×5 ㎛의 면적을 이미지화하였다. 모든 시료는 알코올 처리 및 임계점 건조기(Critical point drying, CPD)를 이용하여 시료 건조 후 표면 분석을 진행하였다.
결과 및 고찰
1. 해조다당류로 네트워크된 콘택트렌즈의 물리적 특성
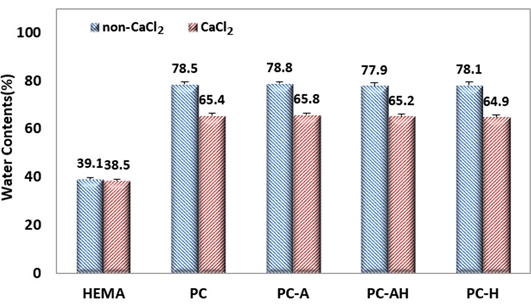
금속이온을 첨가한 시료의 함수율을 Fig. 1에 제시하였다. 발포제가 첨가되지 않은 시료 HEMA를 CaCl2에 담근 후 함수율을 측정한 결과, 함수율의 변화는 나타나지 않았다.
다공성 콘택트렌즈에 칼슘이온을 결합시키면 함수율이 78.15%에서 65.41%로 감소하여 약 19.5% 감소율을 나타내었다. 알긴산과 히알루론산을 첨가한 시료에서도 CaCl2 첨가 시 함수율이 약 19.6~19.9% 감소하였다.
금속이온 첨가 시, 다공성 콘택트렌즈는 함수율이 감소하였으나 비다공성인 HEMA시료는 함수율의 변화가 거의 없었다. 또한 함수율이 천연다당류의 종류에는 영향을 받지 않는 것으로 나타났다.
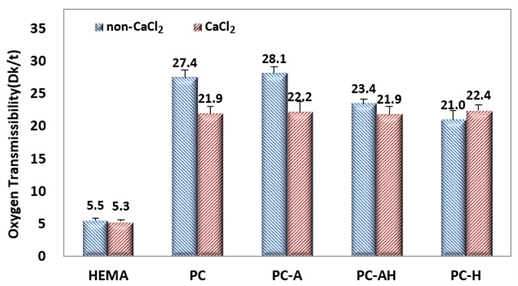
천연다당류와 금속이온이 네트워크된 콘택트렌즈의 산소전달률(Dk/t, cm·mL·O2)/(sec·mL·mmHg)·10-9)은 Fig. 2에 제시하였다.
비다공성의 기본 콘택트렌즈인 HEMA는 칼슘이온을 추가하여도 산소전달률의 변화가 거의 없었다. 또한 다공성 콘택트렌즈에 칼슘이온을 도입하였을 때에는 히알루론산만 첨가한 시료 PC-H를 제외하고 모든 시료에서 산소전달률이 감소하는 경향을 나타내었다. 칼슘이온의 첨가로 시료 PC와 PC-A, PC-AH의 산소전달률이 각각 26.5%, 20.9% 감소하였으며, 칼슘이온이 결합된 PC-H의 Dk/t는 약 7.0% 증가하였다.
금속이온을 첨가하였을 때 산소전달률의 변화량은 PC-A에서 26.5%로 가장 많았으며, 금속이온 첨가로 인해 대부분의 시료에서 산소전달률이 낮아지는 경향을 나타내었다. 이러한 현상은 다당류의 네트워크로 콘택트렌즈 내의 내부 공간이 줄어들었으며, 칼슘이온 첨가로 인한 다당류의 카르복시기와 칼슘이온간의 상호작용으로 내부 공극이 더욱 감소되었기 때문으로 분석한다.
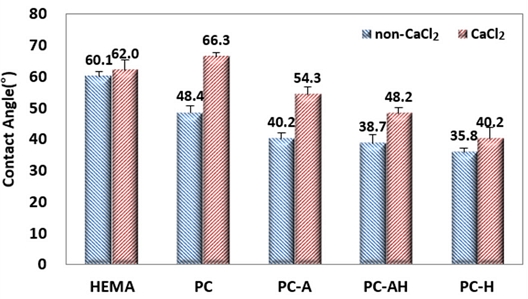
습윤성은 접촉각이 작을수록 좋으며, 본 연구의 접촉각은 Fig. 3에 나타내었다. 비다공성 콘택트렌즈인 HEMA는 칼슘이온이 결합되어도 접촉각의 변화가 나타나지 않았으며, 다공성의 모든 시료에서 접촉각이 증가하는 경향을 내었다. 칼슘이온의 결합으로 인해 PC의 접촉각이 48.4o에서 66.3o로 약 37.0% 증가하였다. 또한 알긴산과 히알루론산을 첨가한 시료에서도 칼슘이온 결합 시에 PC-A, PC-AH 그리고 PC-H의 접촉각이 각각 35.1%, 24.6%, 그리고 12.2%로 증가하였다. 금속이온을 첨가하였을 때, SC가 첨가되어져 있는 시료에만 접촉각의 변화가 일어났으며, 변화량은 천연다당류를 가교하지 않은 시료 PC에서 가장 높게 나타났다. 또한 천연다당류를 가교시킨 시료 중 히알루론산만 첨가했던 시료에서 가장 낮은 변화량을 나타내었다.
일반적으로 천연다당류는 친수성기(-OH)로 인해 습윤성을 가지고 있으며, 습윤성이 높을수록 표면의 거칠기가 낮아지고, 지질 및 단백질의 흡착을 저해시킨다.[25,26] 특히 히알루론산(HA)은 안구환경에 풍부한 glycosamino glycan으로 점탄성 및 전단-박화 특성으로 눈물막 안정성 및 안구 윤활을 향상시키는 것으로 알려져[27] 있기 때문에 히알루론산이 네트워크된 시료의 접촉각이 낮게 나온 것으로 판단된다.
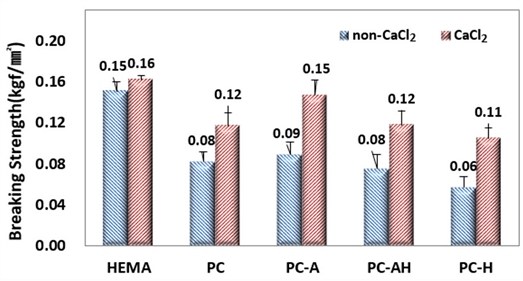
다공성 콘택트렌즈는 일반 콘택트렌즈에 비해 기계적 강도가 낮은 단점이 있다. 따라서 천연다당류로 네트워크시켰으며 칼슘이온을 추가로 네트워크하여 기계적 강도를 보완하였다. 알지네이트와 히알루론산이 네트워크되고 칼슘이온이 추가로 결합된 콘택트렌즈의 파단강도를 측정하여 Fig. 4에 제시하였다.
비다공성 콘택트렌즈인 HEMA는 칼슘이온이 결합되어도 파단강도가 많이 향상되지 않았으나 다공성 콘택트렌즈는 다당류의 네트워크 여부와 상관없이 칼슘이온이 결합되면 파단강도가 많이 향상되었다. PC-A의 칼슘이온 결합 전후 파단강도는 0.089 kgf/㎟에서 0.147 kgf/㎟로 약 65.2% 증가하여 가장 높은 파단강도를 나타냈다. 칼슘이온을 첨가 후 파단강도의 변화는 PC가 약 42.7%, PC-AH는 약 57.3% 그리고 PC-H는 약 84.2%의 증가율로 금속이온첨가 여부에 따라 모든 시료에서 칼슘이온은 파단강도를 향상시켰다. 특히 CaCl2 첨가 전 파단강도가 가장 낮았던 PC-H에서 CaCl2 첨가 후 약 2배가량 가장 높은 증가율을 나타내었지만, 0.105 kgf/㎟로 다른 시료들 보다 여전히 가장 낮은 파단강도를 나타내었다.
천연다당류의 종류에 따른 파단강도를 비교하면, 알지네이트가 포함된 시료가 더 높게 나타났다. 이는 알지네이트는 금속 2가 양이온인 Ca2+ 이온과 “egg-box”를 형성하여 결합력이 향상되었기 때문이다. 칼슘이온이 2개의 알긴산 사슬의 정렬된 G-G 블록 사이에 결합하게 되어 겔화가 형성되었으며, 칼슘이온에 의한 겔화로 인해 탄성 및 기계적 강도가 증가된다는 기존 연구[28]와도 일치한 결과를 나타내었다. 알지네이트가 네트워크된 PC-A는 알지네이트와 히알루론산이 반씩 혼합되어 결합된 PC-AH보다 파단강도가 더 높게 나타난 것도 이러한 이유로 분석된다.
양이온인 칼슘이온은 음의 카르복시기와 직접 이온결합을 형성할 수 있으며,[29] CaCl2가 카르복시 잔기와 반응하여 표면 경도 및 강도를 증가시킨다고 보고하였다.[30]
본 연구에 사용된 다공성 콘택트렌즈 시료에는 알긴산과 히알루론산 뿐만 아니라 친수성 단량체인 MAA가 있으며, MAA에도 카르복실산기가 존재한다. 다공성 콘택트렌즈 내에 MAA의 카르복실산기가 칼슘이온과 가교 결합하여 천연다당류를 포함하는 다공성 하이드로겔 렌즈와 천연다당류를 첨가하지 않은 다공성 하이드로겔 렌즈 모두 기계적 강도가 증가하고 물성이 변한 것으로 판단된다.
2. 천연다당류와 칼슘이온이 결합된 다공성 콘택트렌즈의 단백질 흡착
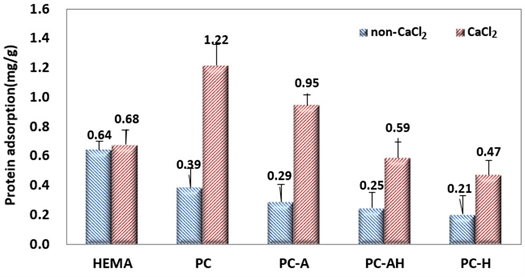
천연다당류와 칼슘이온이 결합된 다공성 콘택트렌즈의 단백질 흡착량은 Fig. 5에 제시하였다. 일반 콘택트렌즈인 HEMA에 비해 다공성 콘택트렌즈는 단백질 흡착이 감소한다. 그러나 칼슘이온이 결합되면 단백질이 많이 흡착되는 것으로 나타났다. CaCl2에 시료를 담근 결과, 발포제가 첨가되지 않은 시료인 HEMA의 단백질 흡착량은 0.642 ㎎/g에서 0.678 ㎎/g으로 큰 변화는 나타나지 않았다. 하지만 발포제가 첨가된 PC의 단백질 흡착량은 0.388 ㎎/g에서 1.216 ㎎/g으로 크게 증가하였다.
PC-A는 CaCl2에 담그기 전과 비교하여 단백질 흡착량이 226.2%, PC-AH는 137.5%, PC-H는 131.2% 증가하였다. 특히 천연다당류를 첨가한 시료 중 히알루론산의 단백질 흡착량이 금속이온을 추가하기 전과 후 모두 가장 낮게 나타났다.
히알루론산이 첨가된 HA-pHEMA의 접촉각은 기존의 pHEMA보다 약 50% 감소된 접촉각을 나타냈으며, 인간혈청알부민(HSA)의 흡착이 감소되었다는 기존 연구[31]와 같이 본 연구에서도 히알루론산의 첨가로 인해 접촉각과 단백질 흡착량이 현저히 감소된 결과를 확인할 수 있었다. 또한 카르복시기(-COOH)의 존재로 인해 음이온성인 알긴산과 히알루론산 모두 음으로 하전된 BSA와 전하 반발에 의해 단백질 흡착이 감소된 것으로 판단된다.
3. 칼슘이온이 결합된 다공성 콘택트렌즈의 표면분석 비교
주사전자현미경을 통해 금속이온을 첨가한 시료의 표면과 단면을 ×3,000로 측정하여 분석한 결과는 Fig. 6에 나타내었다.
다공성 하이드로겔 콘택트렌즈 PC를 CaCl2에 담그기 전과 후의 표면과 단면의 이미지가 다르게 나타났다. 표면의 SEM을 살펴보았을 때, 금속이온을 첨가하지 않은 Fig 6(A)에서는 기공이 원 또는 타원형의 양상을 보였으며, 기공이 없는 부분에는 표면이 매끄럽게 나타났다. 반면에 Fig. 6(B)는 금속이온을 첨가한 표면의 기공이 상대적으로 다각형의 양상을 보였으며, 표면이 거칠게 나타났다.
전자힘현미경(Atomic Force Microscope, AFM)을 통해 살펴본 콘택트렌즈의 표면거칠기를 Fig. 7에 나타내었다.
발포제를 첨가하지 않은 HEMA의 평균 거칠기(Ra)는 금속이온에 담그기 전 0.87±0.012 nm에서 금속이온에 담근 후 0.089±0.004 nm로 변화가 거의 없었다. 그러나 발포제를 첨가한 시료 PC의 평균 거칠기(Ra)는 0.077±0.007 nm에서 0.094±0.014 nm로 22.1% 증가하였으며, 알긴산과 히알루론산을 IPN한 시료 PC-A와 PC-H의 평균 거칠기(Ra)는 금속이온에 담근 후 각각 9.1%, 62.5% 증가하였다.
다공성 하이드로겔 콘택트렌즈는 금속이온의 첨가로 인해 표면의 평균 거칠기(Ra) 값이 모두 증가하는 경향을 나타냈다. 특히 금속이온의 첨가로 인한 표면의 평균 거칠기 값의 증가량이 PC-H에서 가장 높았지만 다른 시료와 비교하였을 때 여전히 가장 낮은 평균 거칠기(Ra)값을 나타냈다.
결 론
다공성 하이드로겔 콘택트렌즈에 천연다당류인 알긴산과 히알루론산을 네트워크하였을 때, 습윤성과 단백질흡착은 크게 향상되었다. 특히 히알루론산은 콘택트렌즈의 함수율과 산소투과율에는 큰 영향을 미치지 않았으나 습윤성과 단백질부착에 대해 많은 영향을 미치는 것을 확인하였다.
콘택트렌즈에 가교된 다당류의 카르복실기와 금속이온이 결합됨으로써 함수율과 산소투과율, 그리고 습윤성을 저하시켰으나, 여전히 다공성 하이드로겔 콘택트렌즈의 높은 물리적 특성을 유지하였다. 또한 금속이온으로 인해 다공성 하이드로겔 콘택트렌즈의 단점인 기계적 강도를 크게 향상시켰다.
다공성 하이드로겔 콘택트렌즈에 도입된 천연다당류는 습윤성 향상 및 단백질 흡착저하 효과를 가져오고, 칼슘이온의 도입으로 강도가 향상됨을 확인하였다.
Acknowledgments
본 연구는 2021년도 정부(교육부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구 사업 (No. 2021R1F1A106332211)으로 연구되었습니다
References
-
Høiby N, Bjarnsholt T, Givskov M, et al. Antibiotic resistance of bacterial biofilms. Int J Amicrob Aents. 2010;35(4): 322-332.
[https://doi.org/10.1016/j.ijantimicag.2009.12.011]

-
Kusuma VA, Gunawan G, Smith ZP, et al. Gas permeability of cross-linked poly(ethylene-oxide) based on poly(ethylene glycol) dimethacrylate and a miscible siloxane co-monomer. Polymer. 2010;51(24):5734-5743.
[https://doi.org/10.1016/j.polymer.2010.09.069]

-
Parsons C, McCoy CP, Gorman SP, et al. Anti-infective photodynamic biomaterials for the prevention of intraocular lens-associated infectious endophthalmitis. Biomater. 2009;30(4):597-602.
[https://doi.org/10.1016/j.biomaterials.2008.10.015]

-
Murakami K, Aoki H, Nakamura S, et al. Hydrogel blends of chitin/chitosan, fucoidan and alginate as healing-impaired wound dressings. Biomater. 2010;31(1):83-90.
[https://doi.org/10.1016/j.biomaterials.2009.09.031]

-
Young MD, Benjamin WJ. Oxygen permeability of the hypertransmissible contact lenses. Eye Contact Lens. 2003;29(1):17-21.
[https://doi.org/10.1097/00140068-200301001-00006]

-
Carney FP, Nash WL, Sentell KB. The adsorption of major tear film lipids in vitro to various silicone hydrogels over time. Investig Ophthalmol Vis Sci. 2008;49(1): 120-124.
[https://doi.org/10.1167/iovs.07-0376]

-
Zhang H, Shi LWE, Zhou J. Recent developments of polysaccharide-based double-network hydrogels. J Polym Sci. 2023;61(1):7-43.
[https://doi.org/10.1002/pol.20220510]

-
Scheuer CA, Fridman KM, Barniak VL, et al. Retention of conditioning agent hyaluronan on hydrogel contact lenses. Cont Lens Anterior Eye. 2010;33(1):2-6.
[https://doi.org/10.1016/j.clae.2010.10.003]

-
Liu Y, Duan LJ, Kim MJ, et al. In situ sodium alginate-hyaluronic acid hydrogel coating method for clinical applications. Macromol Res. 2014;22(3):240-247.
[https://doi.org/10.1007/s13233-014-2001-5]

-
Van Beek M, Jones L, Sheardown H. Hyaluronic acid containing hydrogels for the reduction of protein adsorption. Biomater. 2008;29(7):780-789.
[https://doi.org/10.1016/j.biomaterials.2007.10.039]

-
Singh A, Li P, Beachley V, et al. A hyaluronic acid-binding contact lens with enhanced water retention. Cont Lens Anterior Eye. 2015;38(2):79-84.
[https://doi.org/10.1016/j.clae.2014.09.002]

-
Kumari M, Chauhan GS. Adsorption capacity, kinetics, and mechanism of copper (II) uptake on gelatin?based hydrogels. J Appl Polym Sci. 2011;119(1):363-370.
[https://doi.org/10.1002/app.32632]

-
Wichterle O, Lim D. Hydrophilic gels for biological use. Nature. 1960;185(4706):117-118.
[https://doi.org/10.1038/185117a0]

-
Thakur VK, Thakur MK. Recent trends in hydrogels based on psyllium polysaccharide: a review. J Clean Prod. 2014;82:1-15.
[https://doi.org/10.1016/j.jclepro.2014.06.066]

-
Hamidi M, Azadi A, Rafiei P. Hydrogel nanoparticles in drug delivery. Adv Drug Deliv Rev. 2008;60(15):1638-1649.
[https://doi.org/10.1016/j.addr.2008.08.002]

-
Lin CC, Metters AT. Hydrogels in controlled release formulations: network design and mathematical modeling. Adv Drug Deliv Rev. 2006;58(12-13):1379-1408.
[https://doi.org/10.1016/j.addr.2006.09.004]

-
Shapiro L, Cohen S. Novel alginate sponges for cell culture and transplantation. Biomater. 1997;18(8):583-590.
[https://doi.org/10.1016/S0142-9612(96)00181-0]

-
Rees DA, Welsh EJ, Secondary and tertiary structure of polysaccharides in solutions and gels. Angew Chem Int Ed Engl. 1977;16(4):214-224.
[https://doi.org/10.1002/anie.197702141]

-
Smidsrod O, Skjåk-Braek G. Alginate as immobilization matrix for cells. Trends Biotechnol. 1990;8(3):71-78.
[https://doi.org/10.1016/0167-7799(90)90139-o]

-
Shilpa A, Agrawal SS, Ray AR. Controlled delivery of drugs from alginate matrix. J Macromol Sci Polym Rev. 2003;43(2):187-221.
[https://doi.org/10.1081/MC-120020160]

-
Drury JL, Dennis RG, Mooney DJ. The tensile properties of alginate hydrogels. Biomater. 2004;25(16):3187-3199.
[https://doi.org/10.1016/j.biomaterials.2003.10.002]

-
Prestwich GD, Marecak DM, Marecek JF, et al. Controlled chemical modification of hyaluronic acid: synthesis, applications, and biodegradation of hydrazide derivatives. J Control Release. 1998;53(1-3):93-103.
[https://doi.org/10.1016/S0168-3659(97)00242-3]

-
Park SN, Lee HJ, Lee KH, et al. Biological characterization of EDC-crosslinked collagen–hyaluronic acid matrix in dermal tissue restoration. Biomater. 2003;24(9):1631-1641.
[https://doi.org/10.1016/S0142-9612(02)00550-1]

-
Hilario EC, Stern A, Wang CH, et al. An improved method of predicting extinction coefficients for the determination of protein concentration. PDA J Pharm Sci Technol. 2017;71(2):127-135.
[https://doi.org/10.5731/pdajpst.2016.007120]

-
Tognetto D, Ravalico G. Inflammatory cell adhesion and surface defects on heparin-surface-modified poly(methyl methacrylate) intraocular lenses in diabetic patients. J Cataract Refract Surg. 2001;27(2):239-244.
[https://doi.org/10.1016/s0886-3350(00)00603-9]

-
Gu H, Wang C, Gong S, et al. Investigation on contact angle measurement methods and wettability transition of porous surfaces. Surf Coat Technol. 2016;292:72-77.
[https://doi.org/10.1016/j.surfcoat.2016.03.014]

- Hamano T, Horimoto K, Lee M, et al. Sodium hyaluronate eyedrops enhance tear film stability. Jpn J Ophthalmol. 1996;40(1):62-65.
-
Grant GT, Morris ER, Rees DA, et al. Biological interactions between polysaccharides and divalent cations: the egg-box model. FEBS Lett. 1973;32(1):195-198.
[https://doi.org/10.1016/0014-5793(73)80770-7]

-
Ismail NA, Amin KAM, Razali MH. Preparation of gellan gum(GG) film: the effect of GG, calcium chloride(CaCl2), glycerol concentration and heat treatment. IOP Conf Ser: Mater Sci Eng. 2018;440(1):012006.
[https://doi.org/10.1088/1757-899X/440/1/012006]

-
Shiozawa M, Takahashi H, Iwasaki N, et al. Effect of calcium chloride solution immersion on surface hardness of restorative glass ionomer cements. Dent Mater J. 2013;32(5): 828-833.
[https://doi.org/10.4012/dmj.2013-143]

-
Horkay F, Basser PJ, Londono DJ, et al. Ions in hyaluronic acid solutions. J Chem Phys. 2009;131(18):184902.
[https://doi.org/10.1063/1.3262308]